Moby`s Dicks, Steine und Experimente
Verfasst: 18. Apr 2020, 22:27
Die Mission ist es meine Erfahrungen und die Resultate meiner Arbeit zu teilen.
Sollten an welchem Punkt auch immer Fragen offen stehen, egal ob von Anfänger oder Profi, dann raus damit, ich mache kein Geheimnis aus meinen Methoden!
Ich bin ebenso offen für Anregungen.
Ich starte mit ein Paar vergangenen grows von SWIM, welcher mir den Auftrag gab seine Arbeit hier in der Ich Form zu teilen und werde dann in der nächsten Zeit folgende hinzufügen.
________________________________________
Solltest du einen schlechten Tag haben, vergiss eins nicht - Du kannst einen guten Tag haben und die Kleinigkeiten genießen, den Geruch des Kaffees, die Vögel, die frische Luft, Musik oder was auch immer dich in positiver Weise erregt, ODER du kannst einen schlechten Tag haben und dich von Negativen Emotionen kontrollieren lassen, es ist deine eigene Entscheidung. Übernimm die Kontrolle und hab einen guten Tag.
________________________________________
Mein Bericht startet mit PE6 Multispore auf folgendes high nute Agar Rezept:
250ml Wasser
5g Agar
2g heller Backmalz
1g Dextrose
2,5g Honig
1g Spirulina

Hier ist die Platte eine Weile nachdem sie mit Sporen beimpft wurde.
Dadurch dass das Rezept viele Nährstoffe enthält, ist das Wachstum extrem langsam.
Es sind starke, unterschiedliche Mycelformationen sichtbar, entschieden habe ich mich für die relativ mittige Kultur auf der rechten Seite, weil sie am dicksten, relativ gleichmäßig und groß gewachsen ist.
Die Kultur wurde auf einer neuen Platte vermehrt und zum beimpfen von Roggen (gekocht mit zwei Esslöffeln Gips und circa 1,5 Tassen übrigem Kaffee + rest Wasser) benutzt. Roggen mit Gips zu kochen ist ziemlich ineffizient, weil der Hauptteil im Abfluss landet, also kann man ihn dort weglassen und einfach nur ins bulk mischen.
Von der Platte und der Brut gibt es keine Bilder.
Der spawn (brut) wurde 1:1 mit Kokohum + etwas Gips gebulkt.
Es wird einem überall geraten das bulk substrat auf field capacity zu bewässern, leider wird oft gesagt, dass field capacity bedeutet = 2-3 Tropfen Wasser austretende Flüssigkeit, wenn man das bulk mit der Hand auspresst.
Unser Ziel ist aber so viel wie möglich Wasser im bulk zu haben, also wird maximal bewässert, bis das Coir kein weiteres Wasser mehr halten kann.
Ich sterilisiere grundsätzlich alles, auch das bulk Substrat und Casings.
Nachdem das Bulk sterilisiert wurde, habe ich die Brut gebulkt und mit Folie abgedeckt, um die Kolonisation zu beschleunigen indem der Co2 pegel höher gehalten wird. Außerdem verringert das Abdecken die Verdunstung des Wasser aus dem Substrat, was später den Ertrag verringert.
Hier Flush 1 Erste Generation PE6

Die entstandene Problematik durch das Abdecken war, dass unter der Folie während der Kolonisation des bulks sich eine gute Menge Wasser angesammelt hat.
Ich habe das Wasser nicht abgetupft, sondern die Pfütze in der Mitte gelassen, was zu Cluster pinning in der Mitte geführt hat.
Das Problem wurde in der Nächsten Generation "behoben".
Vom ersten Flush der Ersten Generation habe ich zwei Klone genommen und zwar folgende

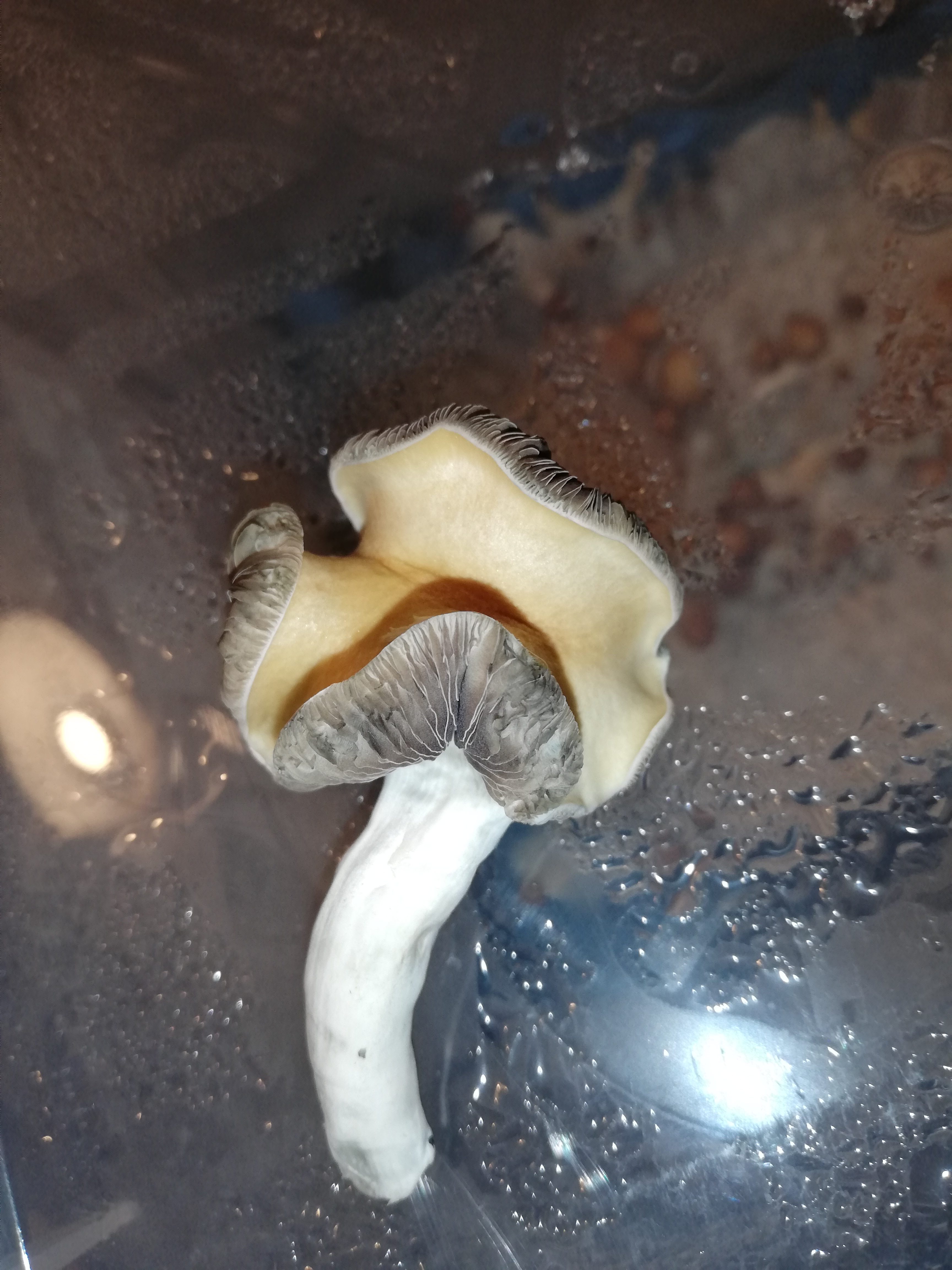

Meine Wahl fiel auf einen mit extrem kurzem Stamm und verhältnismäßig großem Hut, der Hut enthält mehr Magie als der Stamm, also war für mich klar, dass das Klon nummer eins wird.
Der zweite Klon ist ein mutierter wavy cap pheno mit einem zweiten Lamellenring, der außerdem mehr gebläut hat als die anderen.
Beide wurden auf unterschiedliche Platten geklont und damit neuer Roggen beimpft, die Brut beider Klone wurde zusammen im selben tub wieder gefruchtet, dazu aber später mehr, vorher kommt eine weitere PE6 Generation 1 Box.
Bei der folgenden Box wurde das Problem mit der Kondensation unter der Folie mit einem Casing gelöst, das casing hat beim auftragen jegliche Restfeuchtigkeit aufgesaugt und somit das Problem beseitigt.
Mein Casing Rezept besteht aus 50% Weißtorf, 50% Vermikulit und 0,85g Natron pro 300ml Casing Substrat.
Weißtorf ist besonders Nährstoffarm und war außerdem der einzige Torf der nicht zusätzlich vorgedüngt wurde.
Das Casing soll aus zwei Gründen extrem wenige Nährstoffe enthalten.
Grund 1
Kontamination den geringst möglichen Spielraum lassen um auszukeimen und die Box zu versauen, das Casing wird nämlich oftmals nicht zu 100% besiedelt.
Grund 2
Das Casing signalisiert dem Mycel durch den geringen Nährstoffanteil, dass es keine weiteren Nährstoffe zu besiedeln gibt und die Fruchtung eingeleitet werden soll, Stichwort Casing bei Exoten und Trüfflern.
Somit kommen wir zum ersten Vorteil eines Casings, die Fruchtung wird stimuliert und zwar gleichmäßig über die ganze Fläche (wenn das Casing anständig aufgetragen wurde! Darauf werde ich in der nächsten Zeit eingehen, einige Experimente mit Casings habe ich Dokumentiert).
Weitere Vorteile eines Casings sind das Reduzieren der Verdunstung des Wassers im Substrat (Ähnlich wie die Abdeckfolie während das bulk kolonisiert) und zusätzliche Wasserversorgung während der Fruchtung, da wir das Casing während der Fruchtung durch direktes besprühen konstant feucht halten können und das Mycel die zusätzliche Feuchtigkeit für die Fruchtproduktion nutzt, was in erhöhtem Ertrag resultiert.
Das Natron wurde als Alkalischer gegenspieler hinzugefügt. Die Oberfläche den Substrats wird durch das Mycel nach einer Zeit in ein leicht säuerliches Milieu umgewandelt, was Kontaminationen zu gute kommt, diese bevorzugen nämlich saures Milieu, Der Natron arbeitet hier gegen.
Also hier das Ergebnis des 3-4mm dicken Casings aufgetragen nachdem das bulk zu 99% kolonisiert war.

Die Fruchtung hat Gleichmäßig angefangen.

Hier ein bisschen weiter in der Fruchtung.

Und schließlich kurz vor der Ernte

Weil es so schön war noch aus einem anderen Winkel

Und noch einer
Also das ist doch schon ein saftiger Unterschied zur Box die nicht gecased wurde, anmerkung das ist keine Mörder Kultur an der ich vorher Monate gearbeitet habe, es handelt sich um die selbe Kultur wie die andere Box, nämlich ein transfer nach Multispore auf Agar und dann direkt Roggen beimpft.
Eine andere wichtige zu erwähnende Sache ist, bemalt nicht die Boxen von außen oder von innen schwarz in der Hoffnung dadurch Pins am Boden und den Seiten zu verhindern, das bringt fast nichts!
Die schwarze Farbe hemmt lediglich das Licht, welches an den Seiten und am Boden die Fruchtung stimuliert, allerdings ist Licht nicht der einzige Trigger für die Fruchtung.
Wir wollen für maximalen Erfolg IMMER ein ausgeschnittenes Stück Mülltüte in die Box, unter das Substrat und darin dann bulken.
Das Mycel hält sich an der Folie fest wenn es das bulk kolonisiert und genau das wollen wir.
Dadurch, dass das Mycel sich an der Folie festklammert, kann von den Seiten und am Boden kein Wasser verdunsten, was A dafür sorgt, dass wir weniger Wasser verlieren, was dann wieder in geringerem Ertrag resultiert UND außerdem dadurch die Fruchtung von den Seiten und dem Boden verhindert.
Die Feuchtigkeit kann nur nach oben hin durch das Casing entweichen, was zusätzlich für ein deutlich besseres Pinset sorgt.
Wenn die Folie sich schon in Flush eins von den Seiten löst, dann hast du die Folie wahrscheinlich zu Groß geschnitten oder nicht anständig genug das Substrat beim bulken "reingelegt".
Fortsetzung folgt bald
Sollten an welchem Punkt auch immer Fragen offen stehen, egal ob von Anfänger oder Profi, dann raus damit, ich mache kein Geheimnis aus meinen Methoden!
Ich bin ebenso offen für Anregungen.
Ich starte mit ein Paar vergangenen grows von SWIM, welcher mir den Auftrag gab seine Arbeit hier in der Ich Form zu teilen und werde dann in der nächsten Zeit folgende hinzufügen.
________________________________________
Solltest du einen schlechten Tag haben, vergiss eins nicht - Du kannst einen guten Tag haben und die Kleinigkeiten genießen, den Geruch des Kaffees, die Vögel, die frische Luft, Musik oder was auch immer dich in positiver Weise erregt, ODER du kannst einen schlechten Tag haben und dich von Negativen Emotionen kontrollieren lassen, es ist deine eigene Entscheidung. Übernimm die Kontrolle und hab einen guten Tag.
________________________________________
Mein Bericht startet mit PE6 Multispore auf folgendes high nute Agar Rezept:
250ml Wasser
5g Agar
2g heller Backmalz
1g Dextrose
2,5g Honig
1g Spirulina

Hier ist die Platte eine Weile nachdem sie mit Sporen beimpft wurde.
Dadurch dass das Rezept viele Nährstoffe enthält, ist das Wachstum extrem langsam.
Es sind starke, unterschiedliche Mycelformationen sichtbar, entschieden habe ich mich für die relativ mittige Kultur auf der rechten Seite, weil sie am dicksten, relativ gleichmäßig und groß gewachsen ist.
Die Kultur wurde auf einer neuen Platte vermehrt und zum beimpfen von Roggen (gekocht mit zwei Esslöffeln Gips und circa 1,5 Tassen übrigem Kaffee + rest Wasser) benutzt. Roggen mit Gips zu kochen ist ziemlich ineffizient, weil der Hauptteil im Abfluss landet, also kann man ihn dort weglassen und einfach nur ins bulk mischen.
Von der Platte und der Brut gibt es keine Bilder.
Der spawn (brut) wurde 1:1 mit Kokohum + etwas Gips gebulkt.
Es wird einem überall geraten das bulk substrat auf field capacity zu bewässern, leider wird oft gesagt, dass field capacity bedeutet = 2-3 Tropfen Wasser austretende Flüssigkeit, wenn man das bulk mit der Hand auspresst.
Unser Ziel ist aber so viel wie möglich Wasser im bulk zu haben, also wird maximal bewässert, bis das Coir kein weiteres Wasser mehr halten kann.
Ich sterilisiere grundsätzlich alles, auch das bulk Substrat und Casings.
Nachdem das Bulk sterilisiert wurde, habe ich die Brut gebulkt und mit Folie abgedeckt, um die Kolonisation zu beschleunigen indem der Co2 pegel höher gehalten wird. Außerdem verringert das Abdecken die Verdunstung des Wasser aus dem Substrat, was später den Ertrag verringert.
Hier Flush 1 Erste Generation PE6

Die entstandene Problematik durch das Abdecken war, dass unter der Folie während der Kolonisation des bulks sich eine gute Menge Wasser angesammelt hat.
Ich habe das Wasser nicht abgetupft, sondern die Pfütze in der Mitte gelassen, was zu Cluster pinning in der Mitte geführt hat.
Das Problem wurde in der Nächsten Generation "behoben".
Vom ersten Flush der Ersten Generation habe ich zwei Klone genommen und zwar folgende



Meine Wahl fiel auf einen mit extrem kurzem Stamm und verhältnismäßig großem Hut, der Hut enthält mehr Magie als der Stamm, also war für mich klar, dass das Klon nummer eins wird.
Der zweite Klon ist ein mutierter wavy cap pheno mit einem zweiten Lamellenring, der außerdem mehr gebläut hat als die anderen.
Beide wurden auf unterschiedliche Platten geklont und damit neuer Roggen beimpft, die Brut beider Klone wurde zusammen im selben tub wieder gefruchtet, dazu aber später mehr, vorher kommt eine weitere PE6 Generation 1 Box.
Bei der folgenden Box wurde das Problem mit der Kondensation unter der Folie mit einem Casing gelöst, das casing hat beim auftragen jegliche Restfeuchtigkeit aufgesaugt und somit das Problem beseitigt.
Mein Casing Rezept besteht aus 50% Weißtorf, 50% Vermikulit und 0,85g Natron pro 300ml Casing Substrat.
Weißtorf ist besonders Nährstoffarm und war außerdem der einzige Torf der nicht zusätzlich vorgedüngt wurde.
Das Casing soll aus zwei Gründen extrem wenige Nährstoffe enthalten.
Grund 1
Kontamination den geringst möglichen Spielraum lassen um auszukeimen und die Box zu versauen, das Casing wird nämlich oftmals nicht zu 100% besiedelt.
Grund 2
Das Casing signalisiert dem Mycel durch den geringen Nährstoffanteil, dass es keine weiteren Nährstoffe zu besiedeln gibt und die Fruchtung eingeleitet werden soll, Stichwort Casing bei Exoten und Trüfflern.
Somit kommen wir zum ersten Vorteil eines Casings, die Fruchtung wird stimuliert und zwar gleichmäßig über die ganze Fläche (wenn das Casing anständig aufgetragen wurde! Darauf werde ich in der nächsten Zeit eingehen, einige Experimente mit Casings habe ich Dokumentiert).
Weitere Vorteile eines Casings sind das Reduzieren der Verdunstung des Wassers im Substrat (Ähnlich wie die Abdeckfolie während das bulk kolonisiert) und zusätzliche Wasserversorgung während der Fruchtung, da wir das Casing während der Fruchtung durch direktes besprühen konstant feucht halten können und das Mycel die zusätzliche Feuchtigkeit für die Fruchtproduktion nutzt, was in erhöhtem Ertrag resultiert.
Das Natron wurde als Alkalischer gegenspieler hinzugefügt. Die Oberfläche den Substrats wird durch das Mycel nach einer Zeit in ein leicht säuerliches Milieu umgewandelt, was Kontaminationen zu gute kommt, diese bevorzugen nämlich saures Milieu, Der Natron arbeitet hier gegen.
Also hier das Ergebnis des 3-4mm dicken Casings aufgetragen nachdem das bulk zu 99% kolonisiert war.

Die Fruchtung hat Gleichmäßig angefangen.

Hier ein bisschen weiter in der Fruchtung.

Und schließlich kurz vor der Ernte

Weil es so schön war noch aus einem anderen Winkel

Und noch einer
Also das ist doch schon ein saftiger Unterschied zur Box die nicht gecased wurde, anmerkung das ist keine Mörder Kultur an der ich vorher Monate gearbeitet habe, es handelt sich um die selbe Kultur wie die andere Box, nämlich ein transfer nach Multispore auf Agar und dann direkt Roggen beimpft.
Eine andere wichtige zu erwähnende Sache ist, bemalt nicht die Boxen von außen oder von innen schwarz in der Hoffnung dadurch Pins am Boden und den Seiten zu verhindern, das bringt fast nichts!
Die schwarze Farbe hemmt lediglich das Licht, welches an den Seiten und am Boden die Fruchtung stimuliert, allerdings ist Licht nicht der einzige Trigger für die Fruchtung.
Wir wollen für maximalen Erfolg IMMER ein ausgeschnittenes Stück Mülltüte in die Box, unter das Substrat und darin dann bulken.
Das Mycel hält sich an der Folie fest wenn es das bulk kolonisiert und genau das wollen wir.
Dadurch, dass das Mycel sich an der Folie festklammert, kann von den Seiten und am Boden kein Wasser verdunsten, was A dafür sorgt, dass wir weniger Wasser verlieren, was dann wieder in geringerem Ertrag resultiert UND außerdem dadurch die Fruchtung von den Seiten und dem Boden verhindert.
Die Feuchtigkeit kann nur nach oben hin durch das Casing entweichen, was zusätzlich für ein deutlich besseres Pinset sorgt.
Wenn die Folie sich schon in Flush eins von den Seiten löst, dann hast du die Folie wahrscheinlich zu Groß geschnitten oder nicht anständig genug das Substrat beim bulken "reingelegt".
Fortsetzung folgt bald




